Senin, 25 Maret 2013
Pengertian Sistem Koloid
Berbagai Pengertian Sistem Koloid :
Istilah koloid pertama kali diutarakan oleh seorang ilmuwan Inggris, Thomas Graham,
sewaktu mempelajari sifat difusi beberapa larutan melalui membran
kertas perkamen. Graham menemukan bahwa larutan natrium klorida mudah
berdifusi sedangkan kanji, gelatin, dan putih telur sangat lambat atau
sama sekali tidak berdifusi. Zat-zat yang sukar berdifusi tersebut
disebut koloid.. Tahun 1907, Ostwald, mengemukakan istilah system
terdispersi bagi zat yang terdispersi dalam medium pendispersi. Analogi
dalam larutan, fase terdispersi adalah zat terlarut, sedangkan medium
pendispersi adalah zat pelarut. Sistem koloid adalah suatu campuran
heterogen antara dua zat atau lebih di mana partikel-partikel zat yang
berukuran koloid (fase terdispersi) tersebar merata dalam zat lain
(medium pendispersi).
Koloid adalah
suatu bentuk campuran yang keadaannya antara larutan dan suspensi.
Koloid merupakan sistem heterogen, dimana suatu zat "didispersikan" ke
dalam suatu media yang homogen. Ukuran zat yang didispersikan berkisar
dari satu nanometer (nm) hingga satu mikrometer (µm).
Sistem koloid adalah
suatu bentuk campuran yang keadaannya terletak antara larutan dan
suspensi (+Campuran kasar). Sistem koloid ini mempunyai sifat-sifat khas
yang berbeda dari sifat larutan ataupun suspensi. Sistem koloid terdiri
atas fase terdispersi dengan ukuran tertentu dalam medium pendispersi.
Zat yang didispersikan disebut fase terdispersi, sedangkan medium yang
digunakan untuk mendispersikan disebut medium dispersi. Fase terdispersi
bersifat diskontinu (terputus-putus), sedangkan medium dispersi
bersifat kontinyu.
Sistem koloid adalah campuran heterogen,
telah diketahui bahwa terdapat tiga fase, yaitu padat, cair dan gas.
Dari ketiga fase zat ini dapat dibuat sembilan kombinasi campuran fase
zat, tetapi yang dapat membentuk sistem koloid hanya delapan. Kombinasi
campuran fase gas dan fase gas selalu menghasilkan campuran homogen
(satu fase) sehingga tidak dapat membentuk sistem koloid.
Koloid adalah suatu bentuk campuran
yang keadaannya antara larutan dan suspensi. Larutan memiliki sifat
homogen dan stabil. Suspensi memiliki sifat heterogen dan labil.
Sedangkan koloid memiliki sifat heterogen dan stabil. Koloid merupakan
sistem heterogen, dimana suatu zat "didispersikan" ke dalam suatu media
yang homogen. Ukuran zat yang didispersikan berkisar dari satu nanometer
(nm) hingga satu mikrometer (µm).
Koloid adalah suatu campuran zat heterogen
antara dua zat atau lebih di mana partikel-partikel zat yang berukuran
koloid tersebar merata dalam zat lain. Ukuran koloid berkisar antara
1-100 nm ( 10-7 – 10-5 cm ).
Sistem koloid merupakan
suatu bentuk campuran (sistem dispersi) dua atau lebih zat yang
bersifat homogen namun memiliki ukuran partikel terdispersi yang cukup
besar (1 - 100 nm), sehingga terkena efek Tyndall. Bersifat homogen
berarti partikel terdispersi tidak terpengaruh oleh gaya gravitasi atau
gaya lain yang dikenakan kepadanya; sehingga tidak terjadi pengendapan,
misalnya. Sifat homogen ini juga dimiliki olehlarutan, namun tidak
dimiliki oleh campuran biasa (suspensi).
Koloid adalah
campuran yang ukuran partikel zat terdispersi (terlarut) di dalam
koloid, terletak antara suspensi dan larutan sejati. Koloid disebut juga
dispersi koloid atau sistem koloid.sistem koloid terdiri atas fase
terdispersi dan medium pendispersi dengan ukuran tertentu.
Dari berbagai pengertian diatas dapat dimengerti bahwa sistem koloid adalah
suatu bentuk campuran yang keadaannya terletak anatara larutan dan
suspensi. Sistem koloid memiliki ukuran diantara larutan dan suspensi ,
tidak jernih tetapi tidak memisah jika didiamkan, dan tidak dapat
dipisahkan dengan cara penyaringan.
o
Apabila suatu zat dicampur dengan zat lain akan terjadi penyebaran
secara merat dari zat satu ke zat yang lain yang disebut debgan sistem
dispersi.
o Sistem dispersi
adalah pencampuran secara merata antara dua zat atau lebih. Sistem
disperse terdiri dari dua bagian, yaitu fase terdispersi (komponen yang
jumlahnya lebih sedikit) dan pendispersi (komponen yang jumlahnya
banyak). Berdasarkan perbedaan ukuran zat yang terdispersi. Sistem dispersi dibedakan menjadi larutan koloid dan suspensi.
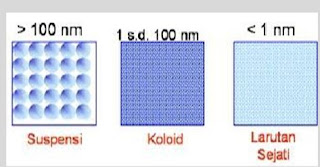
1. Larutan
Larutan
merupakan campuran yang bersifat homogen. Ukuran partikel zat terlarut
di dalam suatu larutan lebih kecil 10-7 (<1nm)>.
2. Suspensi
Suspensi
adalah disperse zat padat dalam air atau campuran heterogen yang
terdiri dari partikel-partikel padat dalam suatu cairan yang bila
dibiarkan akan mengendap ke bawah karena pengaruh gravitasi. Zat
terdispersi pada suspensi merupakan zat padat berukuran cukup besar.
Oleh karena zat terdispersi memiliki ukuran yang cukup besar, medium
pendispersi (air) tidak mampu menahannya sehingga padatan tersebut
mengendap. Ukuran partikel zat yang terdispersi dalam suspensi lebih
besar dari 10-5 cm (> 100 nm) sehingga masih dapat diamati. Contoh :
pasir dilarutkan dalam air.
3. Koloid
Koloid
disebut juga disperse koloid atau suspensi koloid, adalah campuran yang
ukuran partikelnya terletak antara suspensi dan larutan sejati. Ukuran
partikel koloid lebih kecil dibandingkan partikel-partikel suspensi,
tetapi lebih besar dibandingkan partikel-partikel larutan. Ukuran
partikel koloid antara 10-7 - 10-5 cm (1 nm – 100 nm).
Komponen koloid dibagi menjadi dua macam, yaitu :
1. Fase terdispersi
Ø Partikel materi yang tersebar merata dalam suatu medium.
2. Medium pendispersi
Ø Medium partikel ateri yang tersebar.
Perbandingan antara larutan, koloid dan suspensi
| ASPEK | LARUTAN (Dispersi Molekuler) | KOLOID (Dispersi Koloid) | SUSPENSI (Dispersi Kasar) |
| Bentuk campuran | Homogen | Tampak homogen | Heterogen |
| Kestabilan | Stabil | Stabil | Tidak stabil |
| Pengamatan mikroskop | Homogen | Heterogen | Heterogen |
| Jumlah fase | Satu | Dua | Dua |
| Sistem disperse | Molekuler | Padatan halus | Padatan kasar |
| Pemisahan dengan cara penyaringan | Tidak dapat disaring | Tidak dapat disaring dgn kertas saring biasa, kecuali dengan kertas saring ultra | Dapat disaring |
| Ukuran Partikel | <10-7 cm, atau <> | 10-7 cm - 10-5 cm, atau 1 nm - | > 10-5 cm atau > 100 nm |
| Contoh | larutan gula, larutan garam, larutan alkohol, larutan cuka, larutan gas dalam udara, larutan zat yang digunakan dalam laboratorium dan industri | susu, kanji, cat, asap, kabut, buih sabun, dan busa | campuran pasir dengan air, air dengan kopi, minyak dengan air, tanah liat dengan air |
1. Fase terdispersi
Ø Partikel materi yang tersebar merata dalam suatu medium.
2. Medium pendispersi
Ø Medium partikel ateri yang tersebar.
Berikut ini adalah tabel aplikasi koloid:
| Jenis industri | Contoh aplikasi |
| Industri makanan | Keju, mentega, susu, saus salad |
| Industri kosmetika dan perawatan tubuh | Krim, pasta gigi, sabun |
| Industri cat | Cat |
| Industri kebutuhan rumah tangga | Sabun, deterjen |
| Industri pertanian | Peptisida dan insektisida |
| Industri farmasi | Minyak ikan, pensilin untuk suntikan |
SENYAWA HIDROKARBON
SENYAWA HIDROKARBON
Disebut Hidrokarbon : mengandung unsur C dan HTerdiri dari :
1. Alkana (CnH2n+2)
2. Alkena (CnH2n)
3. Alkuna (CnH2n-2)
ALKANA
Hidrokarbon jenuh (alkana rantai lurus dan siklo/cincin alkana)
Disebut golongan parafin : affinitas kecil (=sedikit gaya gabung)
Sukar bereaksi
C1 – C4 : pada t dan p normal adalah gas
C4 – C17 : pada t dan p normal adalah cair
C18 : pada t dan p normal adalah padat
Titik didih makin tinggi : terhadap penambahan unsur C
Jumlah atom C sama : yang bercabang mempunyai TD rendah
Kelarutan : mudah larut dalam pelarut non polar
BJ naik dengan penambahan jumlah unsur C
Sumber utama gas alam dan petroleum
Struktur ALKANA :
CnH2n+2 CH3-CH2-CH2-CH2-CH2-CH3 (heksana)
sikloheksana
PEMBUATAN ALKANA :
Hidrogenasi senyawa Alkena
Reduksi Alkil Halida
Reduksi metal dan asam
PENGGUNAAN ALKANA :
Metana : zat bakar, sintesis, dan carbon black (tinta,cat,semir,ban)
Propana, Butana, Isobutana : zat bakar LPG (Liquified Petrolium Gases)
Pentana, Heksana, Heptana : sebagai pelarut pada sintesis
Fraksi tertentu dari Destilasi langsung Minyak Bumi/mentah
TD (oC) Jumlah C Nama Penggunaan
< 30 1 - 4 Fraksi gas Bahab bakar gas
30 - 180 5 -10 Bensin Bahan bakar mobil
180 - 230 11 - 12 Minyak tanah Bahan bakar memasak
230 - 305 13 - 17 Minyak gas ringan Bahan bakar diesel
305 - 405 18 - 25 Minyak gas berat Bahan bakar pemanas
Sisa destilasi :
1. Minyak mudah menguap, minyak pelumas, lilin dan vaselin
2. Bahan yang tidak mudah menguap, aspal dan kokas dari minyak bumi
ALKENA
Hidrokarbon tak jenuh ikatan rangkap dua
Alkena = olefin (pembentuk minyak)
Sifat fisiologis lebih aktif (sbg obat tidur) : 2-metil-2-butena
Sifat sama dengan Alkana, tapi lebih reaktif
Struktur ALKENA :
CnH2n CH3-CH2-CH=CH2 (1-butena)
ETENA = ETILENA = CH2=CH2
Sifat-sifat : gas tak berwarna, dapat dibakar, bau yang khas, eksplosif dalam udara (pada konsentrasi 3 – 34 %)
Terdapat dalam gas batu bara biasa pada proses “cracking”
Pembuatan : pengawahidratan etanaol
PENGGUNAAN ETENA :
Dapat digunakan sebagai obat bius (dicampur dengan O2)
Untuk memasakkan buah-buahan
Sintesis zat lain (gas alam, minyak bumi, etanol)
PEMBUATAN ALKENA :
Dehidrohalogenasi alkil halida
Dehidrasi alkohol
Dehalogenasi dihalida
Reduksi alkuna
ALKUNA
Hidrokarbon tak jenuh mempunyai ikatan rangkap tiga
Sifat-sifatnya menyerupai alkena, tetapi lebih reaktif
Struktur ALKUNA :
CnH2n-2 CH=CH (etuna/asetilen)
ETUNA = ASETILEN => CH=CH
1. Pembuatan : CaC2 + H2O ------> C2H2 + Ca(OH)2
2. Sifat-sifat :
Suatu senyawaan endoterm, maka mudah meledak
Suatu gas, tak berwarna, baunya khas
3. Penggunaan etuna :
Pada pengelasan : dibakar dengan O2 memberi suhu yang tinggi (+- 3000oC), dipakai
untuk mengelas besi dan baja
Untuk penerangan
Untuk sintesis senyawa lain
PEMBUATAN ALKUNA
Dehidrohalogenasi alkil halida
Reaksi metal asetilida dengan alkil halida primer
SENYAWA AROMATIK
Senyawa alifatis : turunan metana
Senyawa aromatis : turunan benzen (simbol Ar = aril)
Permulaan abad ke-19 ditemukan senyawa-senyawa organik yang mempunyai bau (aroma)
yang karakteristik yang berasal dari tumbuh-tumbuhan (damar benzoin, cumarin, asam
sinamat dll)
BENZEN = C6H6
Senyawa aromatis yang paling sederhana
Berasal dari batu bara dan minyak bumi
Sifat fisika : cairan, td. 80oC, tak berwarna, tak larut dalam air, larut dalam kebanyakan
pelarut organik, mudah terbakar dengan nyala yang berjelaga dan berwarna (karena kadar
C tinggi)
Pengunaan Benzen :
Dahulu sebagai bahan bakar motor
Pelarut untuk banyak zat
Sintesis : stirena, fenol, nilon, anilin, isopropil benzen, detergen, insektisida, anhidrida asam maleat, dsb
ALKIL HALIDA
Senyawa alkil halida merupakan senyawa hidrokarbon baik jenuh maupun tak jenuh yang satu unsur H-nya atau lebih digantikan oleh unsur halogen (X =Br, Cl,I)
Alkil halida = haloalkana = RX struktur primer, sekunder, tersier
Aril halida = ArX = senyawa halogen organik aromatic
Sifat fisika Alkil Halida :
Mempunyai TD lebih tinggi dari pada TD Alkana dengan jumlah unsur C yang sama.
Tidak larut dalam air, tapi larut dalam pelarut organik tertentu.
Senyawa-senyawa bromo, iodo dan polikloro lebih berat dari pada air.
Struktur Alkil Halida :
R-X (X=Br, Cl, I)
CH3-CH2-CH2-CH2-Cl (CH3)2CH-Br (CH3)3C-Br
Primer sekunder tersier
PEMBUATAN ALKIL HALIDA :
Dari alkohol
Halogenasi
Adisi hidrogen halida dari alkena
Adisi halogen dari alkena dan alkuna
PENGGUNAAN ALKIL HALIDA :
Kloroform (CHCl3) : pelarut untuk lemak, obat bius (dibubuhi etanol, disimpan dalam botol
coklat, diisi sampai penuh).
Tetraklorometana = karbontetraklorida (CCl4) : pelarut untuk lemak, alat pemadam
kebakaran (Pyrene, TD rendah 77oC, uapnya berat.
Freon (Freon 12 = CCl2F2, Freon 22 = CHCl2F) : pendingin lemari es, alat “air conditioner”,
sebagai propellant (penyebar) kosmetik, insektisida, dsb.
ALKOHOL
Alkohol : tersusun dari unsur C, H, dan O
Struktur alkohol : R-OH primer, sekunder dan tersier
Sifat fisika alkohol :
TD alkohol > TD alkena dengan jumlah unsur C yang sama (etanol = 78oC, etena =-88,6oC)
Umumnya membentuk ikatan hidrogen
Berat jenis alkohol > BJ alkena
Alkohol rantai pendek (metanol, etanol) larut dalam air (=polar)
Struktur Alkohol : R - OH
R-CH2-OH (R)2CH-OH (R)3C-OH
Primer sekunder tersier
PEMBUATAN ALKOHOL :
Oksi mercurasi – demercurasi
Hidroborasi – oksidasi
Sintesis Grignard
Hidrolisis alkil halide
PENGGUNAAN ALKOHOL :
Metanol : pelarut, antifreeze radiator mobil, sintesis formaldehid,metilamina,metilklorida,metilsalisilat, dll
Etanol : minuman beralkohol, larutan 70 % sebagai antiseptik, sebagai pengawet, dan sintesis eter, koloroform, dll
FENOL
Fenol : mengandung gugus benzen dan hidroksi
Mempunyai sifat asam
Mudah dioksidasi
Mempunyai sifat antiseptik
Penggunaan sbg antiseptikum dan sintesis
ETER
Eter : isomer atau turunan dari alkohol (unsur H pada OH diganti oleh alkil atau aril)
Eter : mengandung unsur C, H, dan O
Sifat fisika eter :
Senyawa eter rantai C pendek berupa cair pada suhu kamar dan TD nya naik dengan
penambahan unsur C.
Eter rantai C pendek medah larut dalam air, eter dengan rantai panjang sulit larut dalam air
dan larut dalam pelarut organik.
Mudah terbakar
Unsur C yang sama TD eter > TD alkana dan < TD alkohol (metil, n-pentil eter 100oC,
n-heptana 98oC, heksil alkohol 157oC).
Struktur eter :
R – O – R CH3-CH2-O-CH2-CH3 (dietil eter)
CH3-CH2-O-C6H5 (fenil etil eter)
PEMBUATAN ETER :
Sintesis Williamson
Alkoksi mercurasi – demercurasi
PENGGUNAAN ETER :
Dietil eter : sbg obat bius umum, pelarut dari minyak, dsb.
Eter-eter tak jenuh : pada opersi singkat : ilmu kedokteran gigi dan ilmu kebidanan.
AMINA
Senyawa organik bersifat basa lemah, dibanding air lebih basa.
Jumlah unsur C kecil sangat mudah larut dalam air.
Sifat fisika Amina :
Suku-suku rendah berbentuk gas.
Tak berwarna, berbau amoniak, berbau ikan.
Mudah larut dalam air
Amina yang lebih tinggi berbentuk cair/padat.
Kelarutan dalam air berkurang dengan naiknya BM.
Struktur amina :
R-NH2, (R)2NH, (R)3N =primer, sekunder, tersier
CH3-CH2-CH2-CH2-NH2 (CH3)2NH (CH3)3N
Primer sekunder tersier
Struktur Amina berdasarkan rantai gugus alkil/aril :
Amina aromatis
Amina alifatis
Amina siklis
Amina campuran
PEMBUATAN AMINA :
Reduksi senyawa nitro
Reaksi alkil halida dengan amonia dan amina
PENGGUNAAN AMINA :
Sebagai katalisator
Dimetil amina : pelarut, absorben gas alam, pencepat vulkanisasi, membuat sabun, dll.
Trimetil amina : suatu penarik serangga.
ALDEHID
Aldehid adalah suatu senyawa yang mengandung gugus karbonil (C=O) yang terikat pada
sebuah atau dua buah unsur hidrogen.
Aldehid berasal dari “ alkohol dehidrogenatum “ (cara sintesisnya).
Sifat-sifat kimia aldehid dan keton umumnya serupa, hanya berbeda dalam derajatnya.
Unsur C kecil larut dalam air (berkurang + C).
Merupakan senyawa polar, TD aldehid > senyawa non polar
Sifat fisika formaldehid : suatu gas yang baunya sangat merangsang
Akrolein = propanal = CH2=CH-CHO : cairan, baunya tajam, sangat reaktif.
FORMALDEHID = METANAL = H-CHO
Sifat-sifat : satu-satunya aldehid yang berbentuk gas pada suhu kamar, tak berwarna,
baunya tajam, larutanya dalam H2O dari 40 % disebut formalin.
Penggunaan : sebagai desinfektans, mengeraskan protein (mengawetkan contoh-contoh
biologik), membuat damar buatan.
Struktur Aldehid :
R – CHO
PEMBUATAN ALDEHID :
Oksidasi dari alkohol primer
Oksidasi dari metilbenzen
Reduksi dari asam klorida
KETON
Keton adalah suatu senyawa organik yang mempunyai sebuah gugus karbonil (C=O) terikat
pada dua gugus alkil, dua gugus aril atau sebuah alkil dan sebuah aril.
Sifat-sifat sama dengan aldehid.
PROPANON = DIMETIL KETON = ASETON = (CH3)2-C=O
Sifat : cairan tak berwarna, mudah menguap, pelarut yang baik.
Penggunaan : sebagai pelarut
ASETOFENON = METIL FENIL KETON
Sifat : berhablur, tak berwarna
Penggunaan : sebagai hipnotik, sebagai fenasil klorida (kloroasetofenon) dipakai sebagai gas
air mata
Struktur :
(R)2-C=O
PEMBUATAN KETON :
Oksidasi dari alkohol sekunder
Asilasi Friedel-Craft
Reaksi asam klorida dengan organologam
ASAM KARBOKSILAT
Mengandung gugus COOH yang terikat pada gugus alkil (R-COOH) maupun gugus aril
(Ar-COOH)
Kelarutan sama dengan alkohol
Asam dengan jumlah C 1 – 4 : larut dalam air
Asam dengan jumlah C = 5 : sukar larut dalam air
Asam dengan jumlah C > 6 : tidak larut dalam air
Larut dalam pelarut organik seperti eter, alkohol, dan benzen
TD asam karboksilat > TD alkohol dengan jumlah C sama.
Struktur Asam Karboksilat :
R – COOH dan Ar – COOH
CH3-CH2-CH2-CH2-COOH : Asam Valerat
CH3-COOH : Asam Asetat
ASAM FORMAT = HCOOH
Sifat fisika : cairan, tak berwarna, merusak kulit, berbau tajam, larut dalam H2O dengan
sempurna.
Penggunaan : untuk koagulasi lateks, penyamakkan kulit, industri tekstil, dan fungisida.
ASAM ASETAT = CH3-COOH
Sifat : cair, TL 17oC, TD 118oC, larut dalam H2O dengan sempurna
Penggunaan : sintesis anhidrat asam asetat, ester, garam, zat warna, zat wangi, bahan
farmasi, plastik, serat buatan, selulosa dan sebagai penambah makanan.
PEMBUATAN ASAM KARBOKSILAT
Oksidasi alkohol primer
Oksidasi alkil benzen
Carbonasi Reagen Grignard
Hidrolisin nitril
AMIDA
Amida adalah turunan asam karboksilat, dimana gugus –OH digan-ti dengan –NH2 atau
amoniak, dimana 1 H diganti dengan asil.
Sifat fisika : zat padat kecuali formamida yang berbentuk cair, tak berwarna, suku-suku
yang rendah larut dalam air, bereaksi kira-kira netral.
Struktur Amida :
R – CONH2
PEMBUATAN AMIDA :
Reaksi asam karboksilat dengan amoniak
Garam amoniumamida dipanaskan
Reaksi anhidrid asam dengan amponiak
PENGGUNAAN AMIDA :
Formamida berbentuk cair, sebagai pelarut.
Untuk identifikasi asam yang berbentuk cair.
Untuk sintesis nilon, dsb.
ESTER
Ester adalah turunan asam karboksilat, dimana gugus H pada –OH diganti dengan gugus R.
Sifat fisika : berbentuk cair atau padat, tak berwarna, sedikit larut dalm H2O, kebanyakan mempunyai bau yang khas dan banyak terdapat di alam.
Struktut ester :
R – COOR
PEMBUATAN ESTER :
Reaksi alkohol dan asam karboksilat
Reaksi asam klorida atau anhidrida
PENGGUNAAN ESTER :
Sebagai pelarut, butil asetat (pelarut dalam industri cat).
Sebagai zat wangi dan sari wangi.
CONTOH – CONTOH SEL VOLTA DALAM KEHIDUPAN SEHARI – HARI
SEL VOLTA
Sel
volta adalah sel elektrokimia yang menghasilkan arus listrik. Sel volta ini
ditemukan oleh dua orang ahli berkebangsaan Italia. Mereka berdua adalah Alessandro
Giuseppe Volta (1745-1827) dan Lugini Galvani (1737-1798).
Ciri khas dari sel volta adalah menggunakan jembatan
garam. Jembatan garam berupa pipa U yang diisi agar-agar yang mengandung
garam kalium klorida. Sel volta terdiri dari anoda yang bermuatan
negatif dan katoda yang bermuatan positif. Pada anoda terjadi proses
oksidasi, oksidasi adalah pelepasan elektron. Sedangkan pada katodanya terjadi
proses reduksi, reduksi adalah penangkapan elektron.
Sel
volta banyak sekali digunakan pada kehidupan sehari-hari. Sel volta yang biasa
digunakan pada kehidupan manusia seperti jenis-jenis baterai dan aki (accu).
Baterai dan aki sangatlah berbeda, perbedaan ini dapat dilihat dari setelah
pemakaian kedua benda tersebut. Baterai apabila sudah terpakai tidak dapat
digunakan lagi karena sudah tidak ada lagi arus listrik pada baterai tersebut.
Sedangkan, aki apabila arus listriknya sudah habis dapat diisi lagi dengan
mengalirkan arus listrik.
Sel volta dibagi menjadi tiga bagian, yaitu Sel
Volta Primer, Sel Volta Sekunder, Sel Bahan Bakar. Ketiga
bagian tersebut juga memiliki contoh masing-masing lagi. Oleh karena itu
marilah kita lihat pembahasan mengenai macam-macam dari sel volta berikut
ini.
v SEL VOLTA PRIMER
a.
Sel
Kering Seng – Karbon
Sel kering juga dapat disebut sel
Lenchanche atau baterai. Baterai kering ini mendapatkan hak paten
penemuan di tahun 1866. Sel Lanchache ini terdiri atas suatu silinder zink
berisi pasta dari campuran batu kawi (MnO2), salmiak (NH4Cl),
karbon (C), dan sedikit air. Dengan adanya air jadi baterai kering ini tidak
100% kering.
Sel
ini biasanya digunakan sebagai sumber tenaga atau energi pada lampu, senter,
radio, jam dinding, dan masih banyak lagi. Penggunaan logam seng adalah sebagai
anoda sedangkan katoda digunakan elektrode inert, yaitu grafit, yang dicelupkan
ditengah-tengah pasta. Pasta ini bertujuan sebagai oksidator. Seng tersebut
akan dioksidasi sesuai dengan persamaan reaksi di bawah ini:
Zn(s) → Zn2+(aq) + 2e-
(anoda)
Sedangkan
katoda terdiri atas campuran dari MnO2 dan NH4Cl. Reaksi
yang terjadi dapat ditulis sebagai berikut:
2MnO2(s) + 2NH4+(aq)
2e- → Mn2O3(s) + 2NH3(aq) + H2O(l)
(katoda)
Katoda
akan menghasilkan ammonia, ammonia ini akan bereaksi dengan Zn2+
yang dihasilkan di anode. Reaksi tersebut akan membentuk ion yang kompleks
[Zn(NH3)4]2+. Sel kering ini tidak dapat
digunakan berulang kali dan memiliki daya tahan yang tidak lama. Dan harganya
di pasaran sangatlah murah.
Baterai merkuri ini merupakan satu
dari baterai kecil yang dikembangkan untuk usaha perdagangan atau komersial.
Anoda seng dan katoda merkuri (II) oksida (HgO) adalah penyusun dari baterai
merkuri ini yang dihubungkan dengan larutan elektrolit kalium hidroksida (KOH).
Sel ini mempunyai beda potensial ± 1,4V. Reaksi yang terjadi pada baterai ini
adalah:
Zn(s) + 2OH-(aq)
→ ZnO(s) + H2O + 2e- (anoda)
HgO(s) + H2O +
2e- → Hg(l) + 2OH-(aq)
(katoda)
Reaksi dari keseluruhan atau disebut reaksi bersih adalah:
Zn(s) + HgO(s)
→ ZnO(s) + Hg(l)
c.
Baterai
Perak Oksida
Baterai perak oksida tergolong tipis
dan harganya yang relatif lebih mahal dari baterai-baterai yang lainnya.
Baterai ini sangat populer digunakan pada jam, kamera, dan kalkulator
elektronik. Perak oksida (Ag2O) sebagai katoda dan seng sebagai
anodanya. Reaksi elektrodenya terjadi dalam elektrolit yang bersifat basa dan
mempunyai beda potensial sama seperti pada baterai alkaline sebesar 1,5V.
Reaksi yang terjadi adalah:
Zn(s) + 2OH-(aq) → Zn(OH)2(s)
+ 2e- (anoda)
Ag2O(s) + H2O + 2e-
→ 2Ag(s) + 2OH-(aq) (katoda)
d.
Baterai
Litium
Terdiri atas litium sebagai anoda
dan MnO2 sebagai oksidator (seperti pada baterai alkaline). Baterai
Litium ini dapat menghasilkan arus listrik yang lebih besar dan daya tahannya
lebih lama dibandingkan baterai kering yang berukuran sama. Berikut notasi dari
baterai Litium:
Li│Li+ (pelarut non-air)│KOH (pasta)│MnO2,
Mn(OH)3, C
v SEL VOLTA SEKUNDER
a.
Aki Timbal
Aki merupakan jenis baterai
yang dapat digunakan untuk kendaran bermotor atau automobil. Aki timbal
mempunyai tegangan 6V atau 12V, tergantung jumlah sel yang digunakan dalam
konstruksi aki timbal tersebut. Aki timbal ini terdiri atas katoda PbO2
(timbel(IV) oksida) dan anodanya Pb (timbel=timah hitam). Kedua zat sel ini
merupakan zat padat, yang dicelupkan kedalam larutan H2SO4.
Reaksi yang terjadi dalam aki adalah:
Pb(s) + SO42-(aq) → PbSO4(s)
+ 2e- (anoda)
PbO2(s) + 4H+(aq) + SO42-(aq)
+ 2e- → PbSO4(s) + 2H2O (katoda)
Aki ini dapat diisi ulang dengan mengalirkan lagi arus listrik ke dalamnya.
Pengisian aki dilakukan dengan membalik arah aliran elektron pada kedua
elektrode. Pada pengosongan aki, anoda (Pb) mengirim elektron ke katoda (PbO2).
Sementara itu pada pengisian aki, elektrode timbal dihubungkan dengan kutub
negatif sumber arus sehingga Pb2SO4 yang terdapat
pada elektrode timbal itu direduksi. Berikut reaksi pengisian aki:
PbSO4(s) + H+(aq) +2e- → Pb(s)
+ HSO4-(aq) (elektrode Pb sebagai
katoda)
PbSO4(s) + 2H2O(l) → PbO2(s)
+ HSO4-(aq) + 3H+(aq) +
2e- (elektrode PbO2 sebagai anoda).
b. Baterai Nikel Kadmium
Baterai nikel-kadmium merupakan
baterai kering yang dapat diisi ulang. Sel ini biasanya disebut nicad
atau bateray nickel-cadmium. Reaksi yang terjadi pada baterai
nikel-kadmium adalah:
Cd(s)
+ 2OH-(aq) → Cd(OH)2(s) + 2e- (anoda)
NiO2(s) + 2H2O + 2e- →
Ni(OH)2(s) + 2OH-(aq) (katoda)
Reaksi
keseluruhan adalah:
Cd(s) + NiO(aq) + 2H2O(l)
→ Cd(OH)2(s) + Ni(OH)2(s)
Baterai nikel-kadmium merupakan zat padat yang melekat pada kedua elektrodenya.
Baterai nikel-kadmium memiliki tegangan sekitar 1,4V. Dengan membalik arah
aliran elektron, zat-zat tersebut dapat diubah kembali seperti zat semula.
c.
Sel Perak Seng
Sel ini mempunyai kuat arus (I) yang besar dan banyak digunakan pada
kendaran-kendaraan balap. Sel perak seng dibuat lebih ringan dibandingkan
dengan sel timbal seng. KOH adalah elektrolit yang digunakan dan elektrodenya
berupa logam Zn (seng) dan Ag (perak).
d.
Sel Natrium Belerang
Sel natrium belerang ini dapat menghasilkan energi listrik yang lebih besar
dari sel perak seng. Elektrodenya adalah Na (natrium) dan S
(sulfur).
e.
Sel
Bahan Bakar
Sel bahan bakar adalah sel
yang menggunakan bahan bakar seperti campuran hidrogen dengan oksigen atau
campuran gas alam dengan oksigen. Sel bahan bakar ini biasanya digunakan untuk
sumber energi listrik pesawat ulang-alik, pesawat Challenger dan Columbia. Yang
berperan sebagai katode adalah gas oksigen dan anodanya gas hidrogen.
Masing-masing elektrode dimasukkan kedalam elektrode karbon yang berpori-pori
dan masing-masingnya elelktrode digunakan katalis dari serbuk platina.
Katoda: menghasilkan ion OH-
O2(g)
+ 2H2O(l) + 4e- → 4OH-(aq)
Anoda: dari katode bereaksi
dengan gas H2
H2(g)
+ 2OH-(aq) → 2H2O(l) + 2e-
Reaksi selnya
adalah: O2(g) + 2H2(g) → 2H2O(l)
SEL VOLTA (SEL GALVANI)
Sel Volta adalah sel elektrokimia yang menghasilkan arus listrik dari
reaksi kimia berupa reaksi redoks spontan. Prinsip kerja sel Volta
adalah sebagai berikut :
1. Energi hasil dari reaksi kini dirubah menjadi energi listrik
2. Reaksi yang berlangsung adalah reaksi redoks
3. Pada katoda terjadi reduksi dan merupakan kutub positif
4. Pada anoda terjadi oksidasi dan merupakan kutub negatif
Jadi katoda positif, Anoda negatif disingkat KPAN yang dibaca KAPAN
KOMPONEN SEL VOLTA
Rangkaian sel elektrokimia pertama kali dipelajari oleh LUIGI GALVANI (1780) dan ALESSANDRO VOLTA (1800). Sehingga disebut sel Galvani atau sel Volta. Keduanya menemukan adanya pembentukan energi dari reaksi kimia tersebut. Energi yang dihasilkan dari reaksi kimia sel Volta berupa energi listrik

Sel Volta terdiri atas elektroda (logam seng dan tembaga) larutan elektrolit (ZnSO4 dan CuSO4), dan jembatan garam (agar-agar yang mengandung KCl). Logam seng dan tembaga bertindak sebagai elektroda. Keduanya dihubungkan melalui sebuah voltmeter. Elektroda tempat berlangsungnya oksidasi disebut Anoda (elektroda negatif), sedangkan elektroda tempat berlangsungnya reduksi disebut Katoda (elektroda positif)
1. Energi hasil dari reaksi kini dirubah menjadi energi listrik
2. Reaksi yang berlangsung adalah reaksi redoks
3. Pada katoda terjadi reduksi dan merupakan kutub positif
4. Pada anoda terjadi oksidasi dan merupakan kutub negatif
Jadi katoda positif, Anoda negatif disingkat KPAN yang dibaca KAPAN
KOMPONEN SEL VOLTA
Rangkaian sel elektrokimia pertama kali dipelajari oleh LUIGI GALVANI (1780) dan ALESSANDRO VOLTA (1800). Sehingga disebut sel Galvani atau sel Volta. Keduanya menemukan adanya pembentukan energi dari reaksi kimia tersebut. Energi yang dihasilkan dari reaksi kimia sel Volta berupa energi listrik

Sel Volta terdiri atas elektroda (logam seng dan tembaga) larutan elektrolit (ZnSO4 dan CuSO4), dan jembatan garam (agar-agar yang mengandung KCl). Logam seng dan tembaga bertindak sebagai elektroda. Keduanya dihubungkan melalui sebuah voltmeter. Elektroda tempat berlangsungnya oksidasi disebut Anoda (elektroda negatif), sedangkan elektroda tempat berlangsungnya reduksi disebut Katoda (elektroda positif)
Elektrokimia
Elektrokimia adalah reaksi redoks yang bersangkut paut dengan listrik.
Reaksi elektrokimia dibagi menjadi 2, yaitu:

Pada gambar di atas, logam Zn akan mengalami oksidasi, sedangkan logam Cu akan mengalami reduksi. Reaksi kimianya adalah:
Seperti pada contoh diatas, berarti notasi selnya adalah:

Sel elektrolisis adalah arus listrik yang menimbulkan reaksi redoks.
Pada sel elektrolisis, katoda akan tereduksi dan anoda yang akan teroksidasi.
Pada katoda, terdapat 2 kemungkinan zat yang ada, yaitu:
Reaksi elektrokimia dibagi menjadi 2, yaitu:
- Sel galvani/sel volta adalah reaksi redoks yang menghasilkan listrik. Contohnya baterai.
- Sel elektrolisis adalah listrik yang mengakibatkan reaksi redoks. Contohnya adalah pemurnian logam dan pelapisan logam.
Sel galvani/sel volta

Pada gambar di atas, logam Zn akan mengalami oksidasi, sedangkan logam Cu akan mengalami reduksi. Reaksi kimianya adalah:
- Zn → Zn2+ + 2 e, E0 = 0,76 volt
- Cu2+ + 2 e → Cu, E0 = 0,34 volt
- Zn + Cu2+ → Zn2+ + Cu, Esel = 1,1 Volt.
Notasi sel
Untuk sel volta, penulisannya adalah: anoda || katoda atau zat yang teroksidasi || zat yang tereduksiSeperti pada contoh diatas, berarti notasi selnya adalah:
- Zn | Zn2+ || Cu2+ | Cu, Esel= 1,1 volt
Sel Elektrolisis

Sel elektrolisis adalah arus listrik yang menimbulkan reaksi redoks.
Pada sel elektrolisis, katoda akan tereduksi dan anoda yang akan teroksidasi.
Pada katoda, terdapat 2 kemungkinan zat yang ada, yaitu:
- kation (K+) atau
- air (H20) (bisa ada atau tidak ada tergantung dari apa yang disebutkan, cairan atau lelehan.)
- anion (A-) atau
- air (H20) (bisa ada atau tidak ada tergantung dari apa yang disebutkan, cairan atau lelehan.)
- elektroda, elektroda ada 2 macam, inert (tidak mudah bereaksi, ada 3 macam zat yaitu platina (Pt), emas (Aurum/Au), dan karbon (C)) dan tak inert (mudah bereaksi, zat lainnya selain Pt, C, dan Au).
- Reaksi yang terjadi pada katoda
- Jika kation merupakan logam golongan IA (Li, Na, K, Rb, Cs, Fr), IIA (Be, Mg, Cr, Sr, Ba, Ra), Al, dan Mn, maka reaksi yang terjadi adalah 2 H20 + 2 e → H2 + 2 OH-
- Jika kationnya berupa H+, maka reaksinya 2H+ + 2 e → H2
- Jika kation berupa logam lain, maka reaksinya (nama logam)x+ + xe → (nama logam)
- Reaksi yang terjadi pada anoda
- Jika elektroda inert (Pt, C, dan Au), ada 3 macam reaksi:
- Jika anionnya sisa asam oksi (misalnya NO3-, SO42-), maka reaksinya 2 H20 → 4H+ + O2 + 4 e
- Jika anionnya OH-, maka reaksinya 4 OH- → 2H20 + O2 + 4 e
- Jika anionnya berupa halida (F-, Cl-, Br-), maka reaksinya adalah 2 X(halida) → X (halida)2 + 2 e
- Jika elektroda inert (Pt, C, dan Au), ada 3 macam reaksi:
-
- Jika elektroda tak inert (selain 3 macam di atas), maka reaksinya Lx+ + xe
Hukum Hess adalah sebuah hukum dalam kimia fisik untuk ekspansi Hess dalam siklus Hess. Hukum ini digunakan untuk memprediksi perubahan entalpi dari hukum kekekalan energi (dinyatakan sebagai fungsi keadaan ΔH).
Hal ini menyebabkan perubahan entalpi suatu reaksi dapat dihitung sekalipun tidak dapat diukur secara langsung. Caranya adalah dengan melakukan operasi aritmatika pada beberapa persamaan reaksi yang perubahan entalpinya diketahui. Persamaan-persamaan reaksi tersebut diatur sedemikian rupa sehingga penjumlahan semua persamaan akan menghasilkan reaksi yang kita inginkan. Jika suatu persamaan reaksi dikalikan (atau dibagi) dengan suatu angka, perubahan entalpinya juga harus dikali (dibagi). Jika persamaan itu dibalik, maka tanda perubahan entalpi harus dibalik pula (yaitu menjadi -ΔH).
Selain itu, dengan menggunakan hukum Hess, nilai ΔH juga dapat diketahui dengan pengurangan entalpi pembentukan produk-produk dikurangi entalpi pembentukan reaktan. Secara matematis
Dengan menggunakan data entalpi pembentukan di atas dapat diketahui perubahan entalpi untuk reaksi-reaksi dibawah ini:
Untuk perubahan entropi:
Penjelasan
Menurut hukum Hess, karena entalpi adalah fungsi keadaan, perubahan entalpi dari suatu reaksi kimia adalah sama, walaupun langkah-langkah yang digunakan untuk memperoleh produk berbeda. Dengan kata lain, hanya keadaan awal dan akhir yang berpengaruh terhadap perubahan entalpi, bukan langkah-langkah yang dilakukan untuk mencapainya.Hal ini menyebabkan perubahan entalpi suatu reaksi dapat dihitung sekalipun tidak dapat diukur secara langsung. Caranya adalah dengan melakukan operasi aritmatika pada beberapa persamaan reaksi yang perubahan entalpinya diketahui. Persamaan-persamaan reaksi tersebut diatur sedemikian rupa sehingga penjumlahan semua persamaan akan menghasilkan reaksi yang kita inginkan. Jika suatu persamaan reaksi dikalikan (atau dibagi) dengan suatu angka, perubahan entalpinya juga harus dikali (dibagi). Jika persamaan itu dibalik, maka tanda perubahan entalpi harus dibalik pula (yaitu menjadi -ΔH).
Selain itu, dengan menggunakan hukum Hess, nilai ΔH juga dapat diketahui dengan pengurangan entalpi pembentukan produk-produk dikurangi entalpi pembentukan reaktan. Secara matematis
 .
.
 .
.
Kegunaan
Hukum Hess menyatakan bahwa perubahan entalpi keseluruhan dari suatu proses hanya tergantung pada keadaan awal dan akhir reaksi, dan tidak tergantung kepada rute atau langkah-langkah diantaranya. Dengan mengetahui ΔHf (perubahan entalpi pembentukan) dari reaktan dan produknya, dapat diramalkan perubahan entalpi reaksi apapun, dengan rumus-
- ΔH=ΔHfP-ΔH fR
-
- ΔH=-ΔHcP+ΔHcR
Contoh umum
Contoh tabel yang digunakan untuk menerapkan hukum Hess| Zat | ΔHfɵ /KJ.mol-1 |
|---|---|
| CH4 (g) | -75 |
| O2 (g) | 0 |
| CO2 (g) | -394 |
| H2O (l) | -286 |
-
- CH4(g)+2O2(g) → CO2(g) + 2H2O(l)
- ΔHcɵ+-75+0=-394+2x-286
- ΔHcɵ-75=-966
- ΔHcɵ=-891KJ.mol-1
Contoh lainnya
Jika diketahui:Persamaan-persamaan reaksi di atas (berikut perubahan entalpinya) dikalikan dan/atau dibalik sedemikian rupa:
- B2O3(s) + 3H2O(g) → 3O2(g) + B2H6(g) ΔH = +2035 kJ
- H2O(l) → H2O(g) ΔH = +44 kJ
- H2(g) + (1/2)O2(g) → H2O(l) ΔH = -286 kJ
- 2B(s) + 3H*2B(s) + (3/2)O2(g) → B2O3(s)
- B2H6(g) + 3O2(g) → B2O3(s) + 3H2O(g) ΔH = -2035 kJ
- 3H2O(g) → 3H2O(l) ΔH = -132 kJ
- 3H2O(l) → 3H2(g) + (3/2)O2(g) ΔH = +858 kJ
- 2B(s) + 3H2(g) → B2H6(g) ΔH = +36 kJ
- 2B(s) + (3/2)O2(g) → B2O3(s) ΔH = -1273 kJ
Untuk perubahan entropi:
- ΔSo = Σ(ΔSfoproduk) - Σ(ΔSforeaktan)
- ΔS = Σ(ΔSoproduk) - Σ(ΔSoreaktan).
- ΔGo = Σ(ΔGfoproduk) - Σ(ΔGforeaktan)
- ΔG = Σ(ΔGoproduk) - Σ(ΔGoreaktan).
Gravimetri
Gravimetri dalam ilmu kimia merupakan salah satu metode kimia analitik untuk menentukan kuantitas suatu zat atau komponen yang telah diketahui dengan cara mengukur berat
komponen dalam keadaan murni setelah melalui proses pemisahan. Analisis
gravimetri melibatkan proses isolasi dan pengukuran berat suatu unsur atau senyawa
tertentu. Metode gravimetri memakan waktu yang cukup lama, adanya
pengotor pada konstituen dapat diuji dan bila perlu faktor-faktor
koreksi dapat digunakan.[1]
Gravimetri dapat digunakan dalam analisis kadar air. Kadar air bahan bisa ditentukan dengan cara gravimetri evolusi langsung ataupun tidak langsung. Bila yang diukur ialah fase padatan dan kemudian fase gas dihitung berdasarkan padatan tersebut maka disebut gravimetri evolusi tidak langsung. Untuk penentuan kadar air suatu kristal dalam senyawa hidrat, dapat dilakukan dengan memanaskan senyawa dimaksud pada suhu 110–130°C. Berkurangnya berat sebelum pemanasan menjadi berat sesudah pemanasan merupakan berat air kristalnya.[2]
Gravimetri dapat digunakan dalam analisis kadar air. Kadar air bahan bisa ditentukan dengan cara gravimetri evolusi langsung ataupun tidak langsung. Bila yang diukur ialah fase padatan dan kemudian fase gas dihitung berdasarkan padatan tersebut maka disebut gravimetri evolusi tidak langsung. Untuk penentuan kadar air suatu kristal dalam senyawa hidrat, dapat dilakukan dengan memanaskan senyawa dimaksud pada suhu 110–130°C. Berkurangnya berat sebelum pemanasan menjadi berat sesudah pemanasan merupakan berat air kristalnya.[2]
Langganan:
Postingan (Atom)